9月2日,复宏汉霖(02696.HK)与Organon(OGN)今日共同宣布,美国食品药品监督管理局(FDA)已批准地舒单抗注射液(60mg/mL)BILDYOS(denosumab-nxxp)和地舒单抗注射液(120mg/1.7mL)BILPREVDA(denosumab-nxxp)的上市申请。两款产品分别为PROLIA(denosumab)和XGEVA(denosumab)的生物类似药,此次获批覆盖原研产品在美国已获批的所有适应症。
截至2025年9月2日收盘,复宏汉霖(02696.HK)报收于77.0港元,下跌3.75%,成交量89.06万股,成交额6940.84万港元。投行对该股的评级以买入为主,近90天内共有4家投行给出买入评级,近90天的目标均价为95.52港元。国投证券股份有限公司最新一份研报给予复宏汉霖买入评级,目标价93.45港元。
机构评级详情见下表:
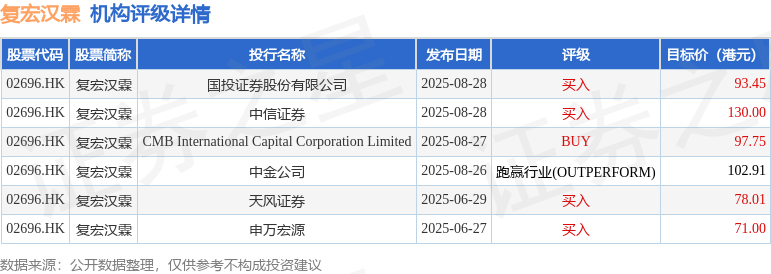
复宏汉霖港股市值130.74亿港元,在生物制品Ⅱ行业中排名第16。主要指标见下表:
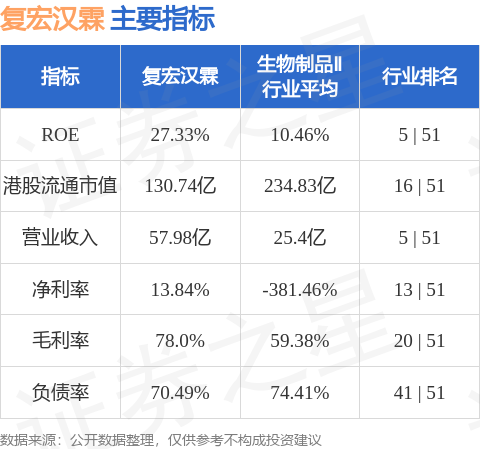
以上内容为证券之星据公开信息整理,由AI算法生成(网信算备310104345710301240019号),不构成投资建议。
